What will be the partial pressure of H2 in a flask containing 2 g of H2, 14 g of N2 and 16 g of O2
(1) 1/2 the total pressure
(2) 1/3 the total pressure
(3) 1/4 the total pressure
(4) 1/16 the total pressure
2 g H2, 14 g N2 और 16 g O2 युक्त एक फ्लास्क में H2 का आंशिक दाब क्या होगा [Assam JET 1992]
(1) 1/2 कुल दाब
(2) 1/3 कुल दाब
(3) 1/4 कुल दाब
(4) 1/16 कुल दाब
The rms velocity of hydrogen is times the rms velocity of nitrogen. If T is the temperature of the gas [IIT 2000]
(1)
(2)
(3)
(4)
हाइड्रोजन का वर्ग माध्य मूल वेग नाइट्रोजन के वर्ग माध्य मूल वेग का गुना है। यदि T गैस का तापमान है तो [IIT 2000]
(1)
(2)
(3)
(4)
A sample of a given mass of a gas at a constant temperature occupies 95cm3 under a pressure of . At the same temperature,find its volume at a pressure of is [Bihar CEE 1992]
(1) 190 cm3
(2) 93 cm3
(3) 46.5 cm3
(4) 47.5 cm3
के दाब में एक स्थिर तापमान पर गैस के दिए गए द्रव्यमान का एक नमूना 95 cm3 अधिग्रहित करता है। उसी तापमान पर, के दाब पर इसका आयतन ज्ञात कीजिए [Bihar CEE 1992]
(1) 190 cm3
(2) 93 cm3
(3) 46.5cm3
(4) 47.5cm3
A closed vessel contains equal number of oxygen and hydrogen molecules. Consider the following statements:
1. The average speed of hydrogen molecules is greater.
2. The two gases have different average energies.
3. Hydrogen molecules strike the walls more often.
4. Weight of hydrogen is th of the weight of oxygen.
Wrong statements are –
(A) 1 and 2
(B) 2 and 3
(C) 1 and 3
(D) 2 and 4
एक बंद बर्तन में समान संख्या में ऑक्सीजन और हाइड्रोजन के अणु होते हैं। निम्नलिखित कथनों पर विचार कीजिए:
1. हाइड्रोजन अणुओं की औसत गति अधिक होती है।
2. दो गैसों में अलग-अलग औसत ऊर्जाएँ होती हैं।
3. हाइड्रोजन अणु दीवारों पर अधिक बार प्रहार करते हैं।
4. हाइड्रोजन का भार ऑक्सीजन के भार का है।
गलत कथन हैं –
(A) 1 और 2
(B) 2 और 3
(C) 1 और 3
(D) 2 और 4
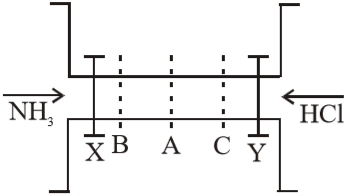
The valves X and Y are opened simultaneously. The white fumes of will first form at :
(1) A
(2) B
(3) C
(4) A, B and C simultaneously
वाल्व X और Y एक साथ खोले जाते हैं। का सफेद धुआँ पहले किस पर बनेगा:
(1) A
(2) B
(3) C
(4) 1, 2 और 3 एक साथ
Given reaction : . Calculate the volume at STP from 48 gm of carbon and excess
(A) 179.2 lit.
(B) 89.6 lit.
(C) 44.8 lit.
(D) 22.4 lit.
दी गई अभिक्रिया है:, 48 g कार्बन और आधिक्य से STP पर आयतन की गणना कीजिए।
(1) 179.2 L
(2) 89.6 L
(3) 44.8 L
(4) 22.4 L
While He is allowed to expand through a small jet under adiabatic condition heating effect is observed. This is due to the fact that:
1. helium is an inert gas
2. helium is a noble gas
3. helium is an ideal gas
4. the inversion temperature of helium is very low
जब He को रूद्धोष्म अवस्था के तहत एक छोटे जेट के माध्यम से विस्तार करने की अनुमति होती है तो तापन प्रभाव देखा जाता है। यह इस तथ्य के कारण है कि:
(1) हीलियम एक अक्रिय गैस है
(2) हीलियम एक उत्कृष्ट गैस है
(3) हीलियम एक आदर्श गैस है
(4) हीलियम का प्रतिलोमी तापमान बहुत कम है
An ideal gas cannot be liquified because
1. its critical temperature is always above 0C
2. its molecules are relatively smaller in size
3. it solidifies before becoming a liquid
4. forces operating between its molecules are negligible
एक आदर्श गैस को द्रवीकृत नहीं किया जा सकता है क्योंकि
(1) इसका क्रांतिक तापमान हमेशा 0C से ऊपर होता है
(2) इसके अणु आकार में अपेक्षाकृत छोटे होते हैं
(3) यह द्रव बनने से पहले ठोस हो जाता है
(4) इसके अणुओं के बीच काम करने वाले बल नगण्य हैं
The temperature at which the r.m.s velocity of carbon dioxide becomes the same as that of nitrogen at 210C is
1. 4620C
2. 273K
3. 1890C
4. 546K
तापमान जिस पर कार्बन डाइऑक्साइड का वर्ग माध्य मूल वेग 210C पर नाइट्रोजन के समान हो जाता है:
1. 4620C
2. 273K
3. 1890C
4. 546K
The volume of 0.0168 mol of O2 obtained by decomposition of KClO3 and collected by displacement of water is 428 ml at a pressure of 754 mm Hg at 25°C. The pressure of water vapour at 25°C is
(1) 18 mm Hg
(2) 20 mm Hg
(3) 22 mm Hg
(4) 24 mm Hg
25°C पर 754 mm Hg के दाब में KClO3 के अपघटन द्वारा प्राप्त O2 के 0.0168 मोल का आयतन और जल के विस्थापन द्वारा एकत्रित 428 ml है। 25°C पर जल वाष्प का दाब है: [UPSEAT 1996]
(1) 18 mm Hg
(2) 20 mm Hg
(3) 22 mm Hg
(4) 24 mm Hg