Four particles have speed 2, 3, 4 and 5 cm/s respectively. Their rms speed is:
1.
2.
3.
4.
चार कणों की क्रमशः गति 2, 3, 4 और 5 cm/s है। उनकी वर्ग माध्य मूल गति है:
1.
2.
3.
4.
A gas occupied a volume of 250 ml at 700 mm Hg pressure and 25°C. What additional pressure is required to reduce the gas volume to its 4/5th value at the same temperature
(1) 225 mm Hg
(2) 175 mm Hg
(3) 150 mm Hg
(4) 265 mm Hg
700 mm Hg दाब और 25°C पर एक गैस ने 250 ml आयतन अधिग्रहीत किया। उसी तापमान पर गैस के आयतन को उसके 4/5 मान तक कम करने के लिए कितने अतिरिक्त दाब की आवश्यकता है?
(1) 225 mm Hg
(2) 175 mm Hg
(3) 150 mm Hg
(4) 265 mm Hg
20 L of SO2 diffuses through a porous partition in 60s. Volume of O2 diffuse under similar condition in 30s will be:-
1. 12.14 L
2. 14.14 L
3. 18.14 L
4. 28.14 L
20 L SO2, 60 s में एक सरंध्र विभाजन के माध्यम से विसरित होता है। समान स्थिति में 30 s में O2 का कितना आयतन विसरित होगा?
1.12.14 L
2.14.14 L
3.18.14 L
4.28.14 L
For a certain gas which deviates a little from ideal behaviour, the values of density, p
were measured at different values of pressure, P. The plot of P/p on the Y–axis versus P on the X–axis was nonlinear and had an intercept on the Y–axis, which was equal to
(1)
(2)
(3) RT
(4)
Where M = molar mass.
एक निश्चित गैस के लिए जो आदर्श व्यवहार से थोड़ा विचलित होती है, घनत्व p का मान दाब P के भिन्न मानों पर मापा गया। X–अक्ष पर P के विरुद्ध Y–अक्ष पर P/p का आरेख अरैखिक था और Y- अक्ष पर एक अंतःखंड था, जो किसके बराबर था
(1)
(2)
(3) RT
(4)
जहाँ M = मोलर द्रव्यमान।
The time taken for a certain volume of a gas ‘X’ to diffuse through a small hole is 2 minutes. It takes 5.65 minutes for oxygen to diffuse under the similar conditions. The molecular weight of ‘X’ is [NCERT 1990]
(1) 8
(2) 4
(3) 16
(4) 32
एक छोटे छिद्र के माध्यम से विसरण के लिए गैस 'X' की निश्चित आयतन के लिए लिया गया समय 2 मिनट है।ऑक्सीजन के लिए समान परिस्थितियों में विसरण के लिए 5.65 मिनट लगते हैं। 'X' का आण्विक भार है [NCERT 1990]
(1) 8
(2) 4
(3) 16
(4) 32
What will be the partial pressure of H2 in a flask containing 2 g of H2, 14 g of N2 and 16 g of O2
(1) 1/2 the total pressure
(2) 1/3 the total pressure
(3) 1/4 the total pressure
(4) 1/16 the total pressure
2 g H2, 14 g N2 और 16 g O2 युक्त एक फ्लास्क में H2 का आंशिक दाब क्या होगा [Assam JET 1992]
(1) 1/2 कुल दाब
(2) 1/3 कुल दाब
(3) 1/4 कुल दाब
(4) 1/16 कुल दाब
The rms velocity of hydrogen is times the rms velocity of nitrogen. If T is the temperature of the gas [IIT 2000]
(1)
(2)
(3)
(4)
हाइड्रोजन का वर्ग माध्य मूल वेग नाइट्रोजन के वर्ग माध्य मूल वेग का गुना है। यदि T गैस का तापमान है तो [IIT 2000]
(1)
(2)
(3)
(4)
A sample of a given mass of a gas at a constant temperature occupies 95cm3 under a pressure of . At the same temperature,find its volume at a pressure of is [Bihar CEE 1992]
(1) 190 cm3
(2) 93 cm3
(3) 46.5 cm3
(4) 47.5 cm3
के दाब में एक स्थिर तापमान पर गैस के दिए गए द्रव्यमान का एक नमूना 95 cm3 अधिग्रहित करता है। उसी तापमान पर, के दाब पर इसका आयतन ज्ञात कीजिए [Bihar CEE 1992]
(1) 190 cm3
(2) 93 cm3
(3) 46.5cm3
(4) 47.5cm3
A closed vessel contains equal number of oxygen and hydrogen molecules. Consider the following statements:
1. The average speed of hydrogen molecules is greater.
2. The two gases have different average energies.
3. Hydrogen molecules strike the walls more often.
4. Weight of hydrogen is th of the weight of oxygen.
Wrong statements are –
(A) 1 and 2
(B) 2 and 3
(C) 1 and 3
(D) 2 and 4
एक बंद बर्तन में समान संख्या में ऑक्सीजन और हाइड्रोजन के अणु होते हैं। निम्नलिखित कथनों पर विचार कीजिए:
1. हाइड्रोजन अणुओं की औसत गति अधिक होती है।
2. दो गैसों में अलग-अलग औसत ऊर्जाएँ होती हैं।
3. हाइड्रोजन अणु दीवारों पर अधिक बार प्रहार करते हैं।
4. हाइड्रोजन का भार ऑक्सीजन के भार का है।
गलत कथन हैं –
(A) 1 और 2
(B) 2 और 3
(C) 1 और 3
(D) 2 और 4
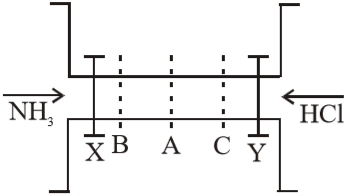
The valves X and Y are opened simultaneously. The white fumes of will first form at :
(1) A
(2) B
(3) C
(4) A, B and C simultaneously
वाल्व X और Y एक साथ खोले जाते हैं। का सफेद धुआँ पहले किस पर बनेगा:
(1) A
(2) B
(3) C
(4) 1, 2 और 3 एक साथ